Pojasnimo, kaj je atom in kako je sestavljen vsak njegov del. Tudi njegova zgodovina, študije o tem in kaj je molekula.

Kaj je atom?
Najmanjša enota, ki sestavlja zadeva.
Beseda atom izvira iz starogrščine (atom, "Brez delitve") in so ga skovali prvi filozofi za teoretizacijo o sestavi stvari, to je o osnovnih delcih vesolje. Od takrat, s pojavom atomski modeli, način njihove predstavitve se je zelo spremenil, saj je atomski model nasledil prejšnjega skozi stoletja, dokler nismo dosegli tistega, ki ga uporabljamo danes.
Atomi imajo lastnosti kemični element ki sestavljajo, elementi pa so organizirani in razvrščeni glede na svoje atomske številke, elektronska konfiguracija in kemijske lastnosti v Periodični sistem elementov.
Isti kemični element je lahko sestavljen iz različnih atomov istega razreda, torej z istim atomskim številom (število protoni ki jih ima vsak atom v elementu), čeprav so njihove atomske mase različne.
Na primer, obstajajo različni atomi istega elementa, ki se razlikujejo po številu nevtroni, in se imenujejo izotopi, reprezentativen primer so izotopi elementa ogljik (12C, 13C, 14C). Torej, vsak atom pripada istemu kemičnemu elementu ali ne, odvisno od njegovega števila protonov, torej atomi z enakim številom protonov pripadajo istemu kemičnemu elementu.
Kako je sestavljen atom?
Atomi so sestavljeni iz jedra in enega ali več elektronov (ki imajo negativen naboj) okoli njega. Jedro je sestavljeno iz delcev, imenovanih protoni in nevtroni. Protoni so pozitivno nabiti, nevtroni pa nevtralni. Nabor protonov in nevtronov se imenuje nukleoni.
Protone in elektrone med seboj privlači elektromagnetna sila (interakcija nabitih delcev z električnim in magnetnim poljem), medtem ko protone in nevtrone privlači jedrska sila (sila, ki jo doživljajo samo delci, ki sestavljajo atomsko jedro).
Kako se atomi združujejo?
Atomi se lahko kombinirajo med seboj in tvorijo kemične povezave, kaj se zgodi, ko si tako ali drugače delijo svoje elektrone. Kemične vezi so lahko kovalentna, ionski Y kovinski, ki izvira iz kovalentnih molekularnih spojin, ionskih mrež ali kovinskih spojin (čeprav je pomembno pojasniti, da nobena kemična vez ni popolnoma kovalentna ali ionska). Na ta način se lahko atomi združijo v tvorbo molekule preprosta kot Voda, kot tudi oblikovati makromolekule kompleksen kot beljakovine, DNK Y RNA.
Čeprav se atomi med seboj razlikujejo zaradi konfiguracije svojih delcev, je tudi res, da so vsi atomi istega elementa popolnoma enaki: atomi vodika v sonce So enaki tistim, ki sestavljajo naše telo, ogljikovi atomi v telesu psa pa so enaki tistim, ki sestavljajo diamant. Razlika je v načinu, kako se atomi združujejo in tvorijo različne kemične spojine, ki sestavljajo organe in organske sisteme v živa bitja, materiali, ustvarjeni v industrijo, in vse snovi, ki sestavljajo vesolje.
Deli atoma
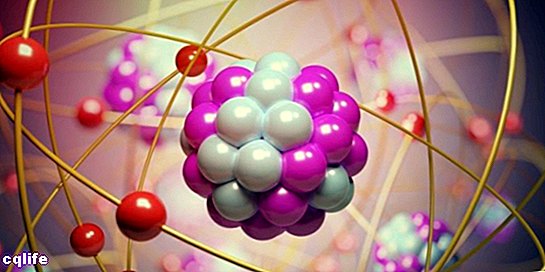
Atomi so sestavljeni iz dveh bistvenih delov:
- Jedro. Približno 99,94 % mase atoma je skoncentriranega v jedru, kjer so protoni in nevtroni (ki jih skupaj imenujemo "nukleoni"), združene z močnimi jedrskimi silami, kar preprečuje, da se protoni, ki se odbijajo drug od drugega, imajo enako električno napolniti.
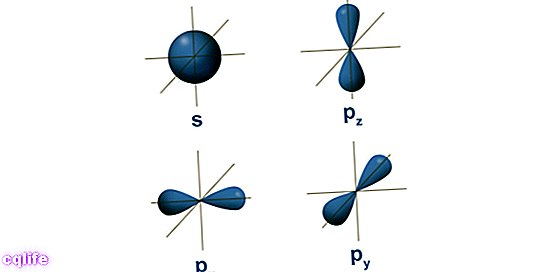
- Atomske orbitale. Orbitala opisuje območje prostora, ki obdaja atomsko jedro, v katerem je verjetnost najti elektron je zelo visoka. Te regije imajo različne oblike, ki jih dobimo kot rezultat reševanja stacionarne Schrödingerjeve enačbe. Erwin Schrödinger je bil avstrijski znanstvenik, ki je razvil to enačbo leta 1925 za izračun razvoja subatomskega delca, kot so elektroni. Tako elektroni tvorijo nekakšen »oblak« okoli jedra, ki ga predstavlja oblika atomskih orbital. Po drugi strani pa vsaka atomska orbitala ustreza določeni energijski vrednosti za elektrone, zato so organizirani glede na njihove energijske vrednosti. Naslednja slika prikazuje oblike prvih atomskih orbital:
Zgodovina atoma

Prvi, ki je oblikoval idejo o obstoju atomov, je bil grški filozof Demokrit (s.V-VI pr.n.št.) iz čisto namišljenih špekulacij (kot so takrat razumeli znanost).
Njegove študije so prevzeli kasnejši filozofi, kot sta Levkip in Epikur, vendar je bil med srednjeveški, v senci kreacionistične razlage sveta, ki je vse pripisovala Bogu.
Počakati smo morali do leta 1773, ko je francoski kemik Antoine de Lavoisier postavil svojo teorijo o neustvarjanju ali uničevanju snovi (le preoblikuje) oz. Zakon ohranjanja mase, kar je Johnu Daltonu omogočilo, da je leta 1804 oblikoval prvo moderno atomsko teorijo.
Zaporedni učenjaki fizično in kemija njegovo delo jih je navdihnilo, da so predlagali boljše in kompleksnejše sisteme za razumevanje temeljnih delcev materije. Kasneje so bili predlagani novi atomski modeli do tistih, ki se danes najbolj uporabljajo.
Sodobna sprejeta struktura je tista, ki izhaja iz poskusi Rutherforda leta 1911, skupaj s formulacijami Nielsa Bohra, Schrödingerja in Heisenberga.
molekula
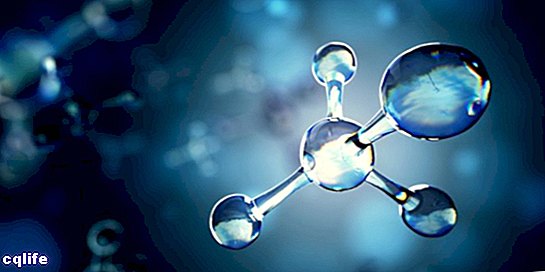
Molekula je znana kot združitev dveh ali več atomov s pomočjo kemičnih vezi, da se tvori bolj zapletena in električno nevtralna struktura. Kemične vezi so lahko kovalentne ali ionske.
Molekule so lahko sestavljene iz atomov istega kemičnega elementa, na primer molekule kisika (O2), ali iz atomov različnih kemičnih elementov, na primer molekule glukoze. Monatomski plini, na primer helij (He), se prav tako štejejo za molekule.

